Руски учени предложиха нов метод на базата на пептиди за борба с устойчиви на антибиотици бактерии. Те откриха така наречения механизъм за насочена коагрегация, който се основава на взаимодействието на пептид, способен да образува фибрили с бактериален протеин, блокирайки неговата активност и инхибирайки растежа на микробите. „Lenta.ru“ разказва подробно за изследванията на молекулярни биолози от Института по теоретична и експериментална биофизика на Руската академия на науките и други научни организации.
Антикризисно средство
Един от основните глобални проблеми на нашето време е антибиотичната криза. Все повече бактерии придобиват резистентност (резистентност) към лекарства, които са били и остават единствената надежда за възстановяване за много пациенти с микробни инфекции. В същото време темпът на поява на пазара на нови ефективни антибиотици изостава от скоростта на разпространение на резистентност поради сложността на разработването на такива лекарства и въвеждането им в производството.
На етап клинични изпитвания вече има само няколко десетки антимикробни лекарства, но те също са разновидности на вече познатите класове антибиотици. Бактериите могат потенциално да развият резистентност към тях много бързо, което прави тези лекарства безполезни. Учените изчисляват, че до 2050 г., поради устойчиви на антибиотици инфекции, причинени от супербактерии,
Сега учени от цял свят работят върху създаването на принципно нови антибактериални лекарства. Например, такива лекарства имат имуномодулиращи свойства, тоест повишават имунитета в борбата срещу инфекцията, други се основават на бактериофаги, тоест вируси, които заразяват бактериални клетки. Едно от обещаващите направления е производството на антимикробни пептиди (АМП), които се състоят от няколко десетки аминокиселинни остатъци. Като цяло, пептидите действат чрез повишаване на пропускливостта на бактериалните мембрани чрез образуване на пори, но съществуват и алтернативни механизми.
Антимикробните пептиди, наречени цекропини, са открити за първи път в хемолимфата на гъсеници на насекоми Hyalophora cecropia. По-късно пептиди са открити в земноводни, бозайници и дори растения. Известно е, че е много по-трудно за бактериите да развият резистентност срещу пептиди, но има редица пречки пред широкото им използване в медицината, например активността in vivo (в живо същество) е по-ниска от тази in vitro (в лабораторни условия).

Снимка: Flickr Майкъл Ходж
Амилоиди срещу микроби
Преди това учените са показали, че амилоидогенните пептиди са способни да инхибират растежа на микробите чрез образуване на агрегати (амилоидни фибрили) с бактериални протеини. Въпреки това, остава неясно как способността за образуване на фибрили е свързана със способността за упражняване на антимикробен ефект. За да изяснят механизма на действие, учените създадоха синтезирани пептиди и тестваха тяхното действие върху редица бактерии, включително Pseudomonas aeruginosa . Рибозомният протеин S1 беше избран като целеви протеин, към който пептидът трябва да се свърже. Това е уникален протеин за бактерии, който изпълнява много жизненоважни функции, включително регулиране на копирането на ДНК в микроорганизмите. Деактивирането му (нокаут) води до неизбежна смърт на бактериалните клетки.Препаратите на базата на амилоидогенни пептиди са в състояние да инхибират растежа на микробите чрез образуване на амилоидни фибрили с важни бактериални протеини
В предишна работа изследователите вече описаха структурата на протеина S1 и откриха интересни характеристики, които не се срещат в други подобни протеини. Например, S1 съдържа няколко идентични домейна, наречени OB-fold. Домейните са специфични региони на протеини, които изпълняват специфични функции. Учените са открили, че броят на домейните в S1 зависи от вида на бактериите. Всички грам-отрицателни бактерии имат шест OB-гънки в S1 протеина и функциите на всяка от тях не са напълно дефинирани.
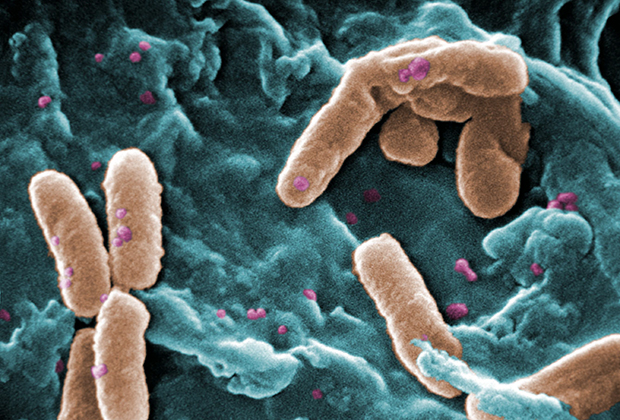
Снимка: Джанис Хейни Кар / CDC
В новата работа изследователите, използващи биоинформатични методи, анализираха домейните на рибозомния протеин S1 от различни видове грам-отрицателни бактерии: E. coli (шест домейна, 557 аминокиселинни остатъци), Thermus thermophilus (пет домейна, 536 аминокиселинни остатъци ) и P. aeruginosa(шест домейна, 559 аминокиселинни остатъка). Целта на работата беше да се идентифицират аминокиселинните последователности на протеин S1, които са склонни към агрегация и сами по себе си могат да имат антибактериални свойства. С други думи, когато се срещат с аналогични аминокиселинни фрагменти, тези региони образуват фибрили, които блокират активността на протеин S1. Важно е, че тези последователности не се намират в еукариотните клетки, така че е изключена възможността пептидите да започнат да образуват агрегати с човешки протеини.
Назад за бъдещето
Въз основа на резултатите от анализа учените синтезират седем амилоидогенни пептида от E. coli , четири пептида от T. thermophilus и четири пептида от P. aeruginosa . За да могат синтезираните пептиди да проникнат през бактериалната мембрана и да се свържат с протеина S1, учените са проектирали модифицирани пептиди с добавяне на специални аминокиселинни последователности, които повишават клетъчната пропускливост.
Сами по себе си, S1 протеините в различни бактерии не образуват амилоидни фибрили; обаче отделни региони наистина образуват агрегати с пептиди. В този случай коагрегацията доведе до образуването на агрегати с различни размери и фибрили с различен диаметър.
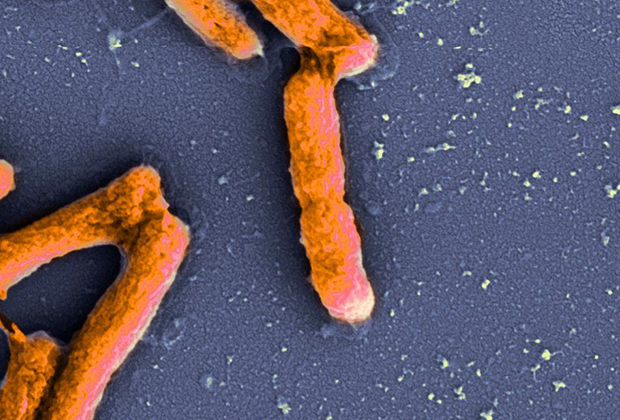
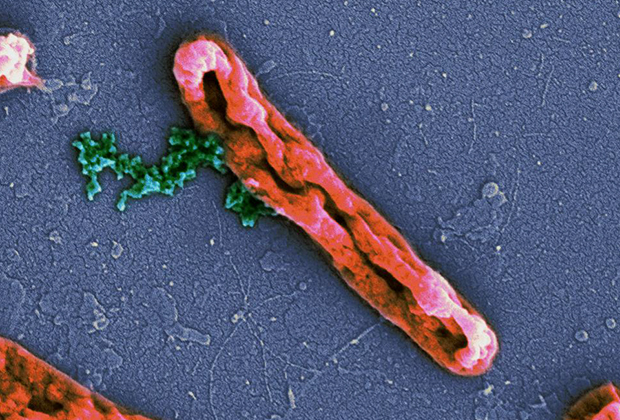


В случай на патогенната бактерия P. aeruginosa, силни антибактериални свойства сред пептидите, синтезирани от предвидените амилоидогенни S1 региони, са открити в пептида R23L, за който минималната инхибиторна концентрация (MIC) е 8 микрограма на милилитър, което е сравнимо с действието на антибиотика гентамицин. Сред пептидите от T. thermophilus S1, най -ефективният пептид е R23I (MIC около 50 микрограма на милилитър), чийто ефект е сравним с антибиотика канамицин. Що се отнася до E. coli, пептидите, базирани на неговия S1 протеин, не са показали същия успех, както в случая на други бактерии. Учените обясняват това с факта, че E. coli има известна резистентност към изследваните пептиди.
По този начин изследователите заключават, че рибозомните протеини S1 на E. coli , T. thermophilus и P. aeruginosa съдържат амилоидогенни последователности, които могат да доведат до агрегация на пептидни молекули помежду си или с други протеини, които имат места на агрегиране. S1-свързани домейни се намират и в други бактериални протеини, което може да увеличи броя на мишените за потенциални пептидни лекарства.
Както пишат авторите на работата, въпреки ниската способност на бактериите да проявяват резистентност към антимикробни пептиди, за да се предотврати и противодейства на появата на нови устойчиви на антибиотици мутанти, е важно да се оцени адаптивната способност на патогенните бактерии към пептиди. Като цяло, механизмът на насочена коагрегация, който се основава на взаимодействието на пептид, способен да образува фибрили с целеви протеин, може да стане основа за нов клас антимикробни лекарства, които могат да решат проблема с антибиотичната резистентност.
Превод и редакция: TRENDY NEWS









